Mitarbeiter
Prof. Dr. Benedikt Kost
Kontakt
- E-Mail: benedikt.kost@fau.de
- Telefon: +49 9131 85-28216
Prof. Dr. Sabine Müller
Kontakt
- E-Mail: sabine.sm.mueller@fau.de
- Telefon: +49 9131 85-28522
PD Dr. Michael Lebert
Privatdozentinnen und Privatdozenten
Kontakt
- E-Mail: michael.lebert@fau.de
Dr.habil. Maria Ntefidou
Wissenschaftliche Mitarbeitende
Kontakt
- E-Mail: maria.ntefidou@fau.de
Dr. Peter Richter
Wissenschaftliche Mitarbeitende
Kontakt
- E-Mail: peter.richter@fau.de
Joline Blaß
Wissenschaftliche Mitarbeitende
Kontakt
- E-Mail: joline.blass@fau.de
Carolin Fritz
Wissenschaftliche Mitarbeitende
Kontakt
- E-Mail: carolin.fritz@fau.de
Johanna Knab
Wissenschaftliche Mitarbeitende
Kontakt
- E-Mail: johanna.knab@fau.de
- Telefon: +49 9131 85-28219
Choy Kriechbaum
Wissenschaftliche Mitarbeitende
Kontakt
- E-Mail: choy.kriechbaum@fau.de
Dr. Sylwia Schulmeister
AG Kost
+49 9131 85 – 28219
sylwia.schulmeister [æt] fau.de
Jennifer Schuster
AG Müller
+49 9131 85 – 28224
jennifer.t.schuster [æt] fau.de
Martin Schuster
AG Kost
+49 9131 85 – 28230
martin.t.schuster [æt] fau.de
Sandra Tauber
AG Kost/AG Müller
+49 9131 85 – 28218 o. 28224
sandra.tauber [æt] fau.de
Hildegard Voll
AG Kost
+49 9131 85 – 28218
hildegard.voll [æt] fau.de
Norbert Meißner
Technischer Sekretär
+49 9131 85 – 28230 o. 28236
norbert.meissner [æt] fau.de
Prof. Dr. Georg Kreimer
georg.kreimer [æt] fau.de
Forschung
Photoorientierung begeißelter Grünalgen
Ziel unserer Forschung ist es die Funktionsweise des Augenfleck-Apparats der Grünalgen, dem „Auge“ dieser Zellen, zu verstehen. Dabei setzen wir eine Kombination aus verschiedenen zellbiologisch und biochemisch- molekularbiologischen Methoden ein. Aufgrund des Vorkommens von Rhodopsinen als Photorezeptoren in einigen Algengruppen und dem komplexen Aufbau dieser photorezeptiven Strukturen wird ihnen eine interessante Rolle bei der Evolution der Lichtwahrnehmung und Verarbeitung zugeschrieben. Die spezialisierten Rhodopsine sind die einzigen bisher bekannten direkt durch Licht aktivierbaren Ionenkanäle. Nach Etablierung der Isolation des Augenfleck-Apparats aus Grünalgen sowie der Charakterisierung des Proteoms und Phosphoproteoms (Schmidt et al. 2006, Plant Cell 18: 1908-1930; Wagner et al. 2008, Plant Physiol. 146: 772-788) interessieren wir uns nun besonders für die von diesem Zellorganell ausgehenden Signaltransduktionswege und die Mechanismen, die für den Zusammenhalt seiner unterschiedlichen subzellulären Komponenten verantwortlich sind. Unser derzeitiger Focus liegt dabei auf der funktionellen Charakterisierung von neuen Ca2+‑bindenden Proteinen sowie der Analyse von Protein-Protein-Interaktionen und Proteinkomplexen. Ein weiterer Schwerpunkt liegt auf der funktionellen Analyse der Photorezeptoren Channelrhodopsin 1 und Phototropin. Hierzu setzen wir unterschiedliche experimentelle Ansätze, wie z.B. RNAi, Phosphorylierungsanalysen, Immunopräzipitation und verschiedene 2D-Elektrophorese-Techniken in Kombination mit Massenspektrometrie, ein.
Als Modell-Organismus verwenden wir hauptsächlich die Grünalge Chlamydomonas reinhardtii. Einige Vorteile dieser Alge, neben denen von Mike Adams hervorgehobenen („Chlamydomonas is pretty, non-pathogenic, doesn´t stink, doesn´t contaminate other cultures and no one cares if you kill it.”), finden Sie hier.
Obwohl eukaryotisch können mikrobielle Standardtechniken bei der Arbeit eingesetzt werden.
Autothrophes, heterotrophes oder mixotrophes Wachstum in definierten Medien oder auf Agar ist möglich. Die Kultur ist einfach und es können schnell größere Mengen herangezogen werden. Unsere Anzucht-Möglichkeiten erlauben z.B. die Kultur von bis zu 100 L pro Woche unter sterilen Bedingungen.
Das Wachstum kann bei Bedarf synchronisiert werden.
C. reinhardtii kann sich sowohl vegetativ als auch geschlechtlich vermehren. Die geschlechtliche Vermehrung kann gezielt durch N-Mangel und Blaulicht induziert werden.
C. reinhardtii ist genetisch gut charakterisiert. Alle drei Genome (Kern, Chloroplast, Mitochondrium) sind bekannt und können mit sehr einfachen Techniken stabil transformiert werden. Entsprechend gibt es eine Vielzahl von Mutanten.
Eine Vielzahl von Mutanten, BAC- und cDNA-Banken, DNA-Chips etc. kann über das Chlamydomonas Center in den USA bezogen werden.
Die Zellen sind motil und zu komplexen Informationsverarbeitungen fähig. Ihr Verhalten kann relativ einfach analysiert werden.
Etliche Proteine weisen höhere Homologien zu Säugern anstatt zu Höheren Pflanzen auf. Somit ist C. reinhardtii beispielsweise auch ein Model für einige humane Krankheiten.
Einen Eindruck von dem Aufbau des Augenfleck-Apparats gibt Abbildung 1. Die ~ 1 µm2 große Struktur kommt in Einzahl in den Zellen vor und kann wegen der starken Anreicherung von Carotenoiden leicht lichtmikroskopisch erkannt werden. Detaillierte ultrastrukturelle und biophysikalische Untersuchungen haben gezeigt, dass der funktionelle Augenfleck-Apparat aus Bestandteilen mehrerer, subzellulärer Kompartimente besteht.
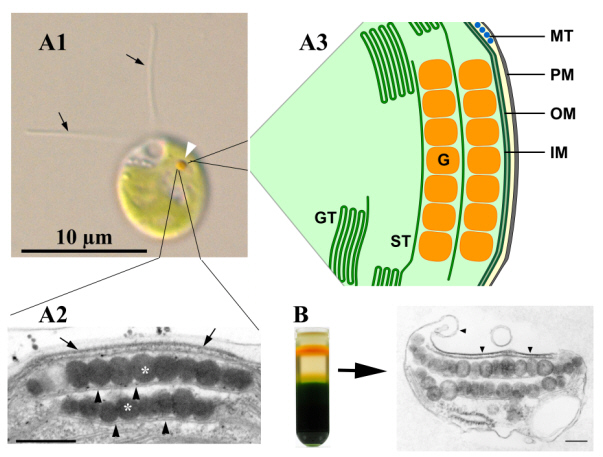
Abb. 1: Der Augenfleck-Apparat von Chlamydomonas reinhardtii im lichtmikroskopischen Bild (A1, weiße Pfeilspitze), im transmissionselektronenmikroskopischen Bild (A2) und im Schema (A3). Strukturell intakte Augenfleck-Apparate können mittels Saccharose-Gradientenzentrifugation isoliert werden (B).
Auffälligster Bestandteil sind hexagonal angeordnete Lagen carotenoidreicher Lipid-Globuli innerhalb des Chloroplasten, die mit je einem Thylakoid assoziiert sind. Die äußerste Globuli-Schicht ist zusätzlich mit spezialisierten Bereichen der Chloroplasten-Hüllmembran und der Plasmamembran verbunden, sodass diese gesamte Einheit isoliert werden kann (siehe Abb. 1B). In den Bereichen der Plasmamembran und der äußeren Chloroplasten-Hüllmembran, die den Globuli aufliegen, ist eine hohe Dichte von Intramembranpartikeln feststellbar. Die biophysikalische und sensorische Funktionsweise des Augenfleck-Apparats ist eng an die Bewegung der Zellen gekoppelt. Letztlich erlaubt diese Struktur in Kombination mit der Schwimmbewegung der Zelle eine exakte Bestimmung der Licht-Richtung und Intensität. Gleichzeitig dient sie zur maximalen Kontrastverstärkung des Lichtsignals am Sitz der Rhodopsine in der Plasmamembran. In letzter Zeit häufen sich daneben Hinweise, dass der Augenfleck-Apparat neben der Lichtwahrnehmung noch weitere wichtige Funktionen innehaben könnte.
Eine detaillierte Beschreibung der Struktur und Funktion dieses „Auges“ der Grünalgen finden Sie in folgendem Übersichtsartikel (Kreimer 2009, Curr. Genet. 55,19-43).
Publikationen
Bücher
- Kreimer, G., Wakabayashi, K.I., Hegemann, P., & Dieckmann, C. (2023). The eyespot and behavioral light responses. Elsevier.
BibTeX: Download
Beiträge in Fachzeitschriften
- Wolfram, M., Greif, A., Baidukova, O., Voll, H., Tauber, S., Lindacher, J.,... Kreimer, G. (2024). Insights into degradation and targeting of the photoreceptor channelrhodopsin-1. Plant Cell and Environment. https://doi.org/10.1111/pce.15017
BibTeX: Download - Wolfram, M., Greif, A., Sizova, I., Baidukova, O., Hegemann, P., & Kreimer, G. (2023). Multifactorial in vivo regulation of the photoreceptor channelrhodopsin-1 abundance. Plant Cell and Environment. https://doi.org/10.1111/pce.14657
BibTeX: Download - Böhm, M., Boness, D., Fantisch, E., Erhard, H., Frauenholz, J., Kowalzyk, Z.,... Kreimer, G. (2019). Channelrhodopsin-1 phosphorylation changes with phototactic behavior and responds to physiological stimuli in Chlamydomonas. The Plant Cell. https://doi.org/10.1105/tpc.18.00936
BibTeX: Download - Greiner, A., Kelterborn, S., Evers, H., Kreimer, G., Sizova, I., & Hegemann, P. (2017). Targeting of Photoreceptor Genes in Chlamydomonas reinhardtii via Zinc-finger Nucleases and CRISPR/Cas9. The Plant Cell, 29(10), 2498-2518. https://doi.org/10.1105/tpc.17.00659
BibTeX: Download - Trippens, J., Reißenweber, T., & Kreimer, G. (2017). The chloroplast Calcium Sensor protein CAS affects phototactic behaviour in Chlamydomonas reinhardtii (Chlorophyceae) at low light intensities. Phycologia, 56(3), 261-270. https://doi.org/10.2216/16-67.1
BibTeX: Download - Eitzinger, N., Wagner, V., Weisheit, W., Geimer, S., Boness, D., Kreimer, G., & Mittag, M. (2015). Proteomic Analysis of a Fraction with Intact Eyespots of Chlamydomonas reinhardtii and Assignment of Protein Methylation. Frontiers in Plant Science, 6. https://doi.org/10.3389/fpls.2015.01085
BibTeX: Download - Schulze, T., Schreiber, S., Iliev, D., Boesger, J., Trippens, J., Kreimer, G., & Mittag, M. (2013). The Heme-Binding Protein SOUL3 of Chlamydomonas reinhardtii Influences Size and Position of the Eyespot. Molecular Plant, 6(3), 931-944. https://doi.org/10.1093/mp/sss137
BibTeX: Download - Trippens, J., Greiner, A., Schellwat, J., Neukam, M., Rottmann, T., Lu, Y.,... Kreimer, G. (2012). Phototropin Influence on Eyespot Development and Regulation of Phototactic Behavior in Chlamydomonas reinhardtii. The Plant Cell, 24(11), 4687-4702. https://doi.org/10.1105/tpc.112.103523
BibTeX: Download - Rolland, N., Atteia, A., Decottignies, P., Garin, J., Hippler, M., Kreimer, G.,... Wagner, V. (2009). Chlamydomonas proteomics. Current Opinion in Microbiology, 12(3), 285-291. https://doi.org/10.1016/j.mib.2009.04.001
BibTeX: Download - Kreimer, G. (2009). The green algal eyespot apparatus: a primordial visual system and more? Current Genetics, 55(1), 19-43. https://doi.org/10.1007/s00294-008-0224-8
BibTeX: Download - Wagner, V., Ullmann, K., Mollwo, A., Kaminski, M., Mittag, M., & Kreimer, G. (2008). The phosphoproteome of a Chlamydomonas reinhardtii eyespot fraction includes key proteins of the light signaling pathway. Plant Physiology, 146(2), 772-788. https://doi.org/10.1104/pp.107.109645
BibTeX: Download - Wagner, V., Kreimer, G., & Mittag, M. (2008). The power of functional proteomics: Components of the green algal eyespot and its light signaling pathway(s). Plant Signaling & Behavior, 3(7), 433-435. https://doi.org/10.4161/psb.3.7.5685
BibTeX: Download - Kreimer, G. (2007). Evidence for a specialized localization of the chloroplast ATP-synthase subunits alpha, beta, and gamma in the eyespot apparatus of Chlamydomonas reinhardtii (Chlorophyceae). Journal of Phycology, 43(2), 284-294. https://doi.org/10.1111/j.1529-8817.2007.00331.x
BibTeX: Download - Kreimer, G. (2006). Proteomic analysis of the eyespot of Chlamydomonas reinhardtii provides novel insights into its components and tactic movements. The Plant Cell, 18(8), 1908-1930. https://doi.org/10.1105/tpc.106.041749
BibTeX: Download - Kreimer, G. (2006). Toward a protein map of the green algal eyespot: analysis of eyespot globule-associated proteins. Phycologia, 45(2), 199-212.
BibTeX: Download - Renninger, S., Backendorf, E., & Kreimer, G. (2001). Subfractionation of eyespot apparatuses from the green alga |Spermatozopsis similis|: Isolation and characterization of eyespot globules. Planta, 213, 51-63. https://dx.doi.org/10.1007/s004250000473
BibTeX: Download - Hill, K., Hemmler, R., Kovermann, P., Calenberg, M., Kreimer, G., & Wagner, R. (2000). A Ca2+- and voltage-modulated flagellar ion channel is a component of the mechanoshock response in the unicellular green alga Spermatozopsis similis. Biochimica Et Biophysica Acta-Biomembranes, 1466(1-2), 187-204. https://dx.doi.org/10.1016/S0005-2736(00)00200-5
BibTeX: Download - Dole, V., Jakubzik, C.R., Brünjes, B., & Kreimer, G. (2000). A cDNA from the green alga Spermatozopsis similis encodes a protein with homology to the newly discovered Roadblock/LC7 family of dynein-associated proteins. Gene Structure and Expression, 1490(1-2), 125-130. https://dx.doi.org/10.1016/S0167-4781(99)00220-1
BibTeX: Download - Kreimer, G. (1999). Reflective properties of different eyespot types in dinoflagellates. Protist, 150, 311-323. https://dx.doi.org/10.1016/S1434-4610(99)70032-5
BibTeX: Download - Calenberg, M., Brohsonn, U., Zedlacher, M., & Kreimer, G. (1998). Light- and Ca2+-modulated heterotrimeric GTPases in the eyespot apparatus of a flagellate green alga. The Plant Cell, 10(1), 91-103. https://dx.doi.org/10.1105/tpc.10.1.91
BibTeX: Download - Santos, L.M.A., Melkonian, M., & Kreimer, G. (1996). A combined reflection confocal laser scanning, electron and fluorescence microscopy analysis of the eyespot in zoospores of Vischeria spp. (Eustigmatales, Eustigmatophyceae). Phycologia, 35(4), 299-307. https://dx.doi.org/10.2216/i0031-8884-35-4-299.1
BibTeX: Download - Kreimer, G. (1996). Light reception and signal modulation during photoorientation of flagellate green algae. Photochemistry and Photobiology, 63(1), 62-63.
BibTeX: Download - Schlicher, U., Linden, L., Calenberg, M., & Kreimer, G. (1995). G proteins and Ca2+-modulated protein kinases of a plasma membrane-enriched fraction and isolated eyespot apparatuses of Spermatozopsis similis (Chlorophyceae). European Journal of Phycology, 30(4), 319-330. https://dx.doi.org/10.1080/09670269500651111
BibTeX: Download - Linden, L., & Kreimer, G. (1995). Calcium modulates rapid protein phosphorylation/dephosphorylation in isolated eyespot apparatuses of the green alga Spermatozopsis similis. Planta, 197(2), 343-351. https://dx.doi.org/10.1007/BF00202656
BibTeX: Download - Kreimer, G. (1995). Flagellar Shock Responses in Green Algae. Botanica Acta : Berichte der Deutschen Botanischen Gesellschaft, 108(3), 169-171. https://dx.doi.org/10.1111/j.1438-8677.1995.tb00847.x
BibTeX: Download - Calenberg, M., Linden, L., & Kreimer, G. (1995). Ca2+ stimulated protein kinases and G-proteins are enriched in both, a plasma membrane fraction and isolated eyespot apparatuses of a green alga. European Journal of Cell Biology.
BibTeX: Download - Höning, S., Kreimer, G., Robenek, H., & Jockusch, B.M. (1994). Receptor-mediated endocytosis is sensitive to antibodies against the uncoating ATPase (hsc70). Journal of Cell Science, 107, 1185-1196.
BibTeX: Download - Grung, M., Kreimer, G., Calenberg, M., Melkonian, M., & Liaaen-Jensen, S. (1994). Carotenoids in the eyespot apparatus of the flagellate green alga Spermatozopsis similis: Adaptation to the retinal-based photoreceptor. Planta, 193(1), 38-43. https://dx.doi.org/10.1007/BF00191604
BibTeX: Download - Kreimer, G., & Witman, G.B. (1994). Novel touch-induced, Ca2+-dependent phobic response in a flagellate green alga. Cell Motility and the Cytoskeleton, 29(2), 97-109. https://dx.doi.org/10.1002/cm.970290202
BibTeX: Download - Hesse, T., Garbers, C., Brzobohaty, B., Kreimer, G., Söll, D., Melkonian, M.,... Palme, K. (1993). Two members of the ERabp gene family are expressed differentially in reproductive organs but to similar levels in the coleoptile of maize. Plant Molecular Biology, 23(1), 57-66. https://dx.doi.org/10.1007/BF00021419
BibTeX: Download - Kreimer, G., Overländer, C., Sineshchekov, O.A., Stolzis, H., Nultsch, W., & Melkonian, M. (1992). Functional analysis of the eyespot in Chlamydomonas reinhardtii mutant ey 627, mt−. Planta, 188(4), 513-521. https://dx.doi.org/10.1007/BF00197043
BibTeX: Download - Kreimer, G., Marner, F.-J., Brohsonn, U., & Melkonian, M. (1991). Identification of 11-cis and all-trans-retinal in the photoreceptive organelle of a flagellate green alga. Febs Letters, 293(1-2), 49-52. https://dx.doi.org/10.1016/0014-5793(91)81150-7
BibTeX: Download - Kreimer, G., Brohsonn, U., & Melkonian, M. (1991). Isolation and partial characterization of the photoreceptive organelle for phototaxis of a flagellate green alga. European Journal of Cell Biology, 55(2), 318-327.
BibTeX: Download - Höning, S., Jockusch, B.M., Kreimer, G., Veltel, D., Robenek, H., Engelhardt, W., & Frey, J. (1991). Endocytosis of human IgG: Fc receptor complexes by transfected BHK cells. European Journal of Cell Biology, 55(1), 48-59.
BibTeX: Download - Katsaros, C., Kreimer, G., & Melkonian, M. (1991). Localization of Tubulin and a Centrin-Homologue in Vegetative Cells and Developing Gametangia of Ectocarpus siliculosus (Dillw.) Lyngb. (Phaeophyceae, Ectocarpales) - A combined immunofluorescence and confocal laser scanning microscope study. Botanica Acta : Berichte der Deutschen Botanischen Gesellschaft, 104(2), 87-92. https://dx.doi.org/10.1111/j.1438-8677.1991.tb00201.x
BibTeX: Download - Kreimer, G., Kawai, H., Müller, D.G., & Melkonian, M. (1991). Reflective properties of the stigma in male gametes of Ectocarpus siliculosus (Phaeophyceae) studied by confocal laser scanning microscopy. Journal of Phycology, 27(2), 268-276. https://dx.doi.org/10.1111/j.0022-3646.1991.00268.x
BibTeX: Download - Kreimer, G., & Melkonian, M. (1990). Reflection confocal laser scanning microscopy of eyespots in flagellated green algae. European Journal of Cell Biology, 53(1), 101-111.
BibTeX: Download - Kreimer, G., Melkonian, M., Holtum, J.A.M., & Latzko, E. (1988). Stromal Free Calcium Concentration and Light-Mediated Activation of Chloroplast Fructose-1,6-Bisphosphatase. Plant Physiology, 86(2), 423-428. https://dx.doi.org/10.1104/pp.86.2.423
BibTeX: Download - Surek, B., Kreimer, G., Melkonian, M., & Latzko, E. (1987). Spinach ferredoxin is a calcium-binding protein. Planta, 171(4), 565-568. https://dx.doi.org/10.1007/BF00392307
BibTeX: Download - Kreimer, G., Surek, B., Woodrow, I.E., & Latzko, E. (1987). Calcium binding by spinach stromal proteins. Planta, 171(2), 259-265. https://dx.doi.org/10.1007/BF00391103
BibTeX: Download - Heimann, K., Kreimer, G., Melkonian, M., & Latzko, E. (1987). Light-Induced Ca2+ Influx into Spinach Protoplasts. Zeitschrift für Naturforschung Section C - A Journal of Biosciences, 42(3), 283-287.
BibTeX: Download - Kreimer, G., Melkonian, M., & Latzko, E. (1985). An electrogenic uniport mediates light-dependent Ca2+ influx into intact spinach chloroplasts. Febs Letters, 180(2), 253-258. https://dx.doi.org/10.1016/0014-5793(85)81081-4
BibTeX: Download - Kreimer, G., Melkonian, M., Holtum, J.A.M., & Latzko, E. (1985). Characterization of calcium fluxes across the envelope of intact spinach chloroplasts. Planta, 166(4), 515-523. https://dx.doi.org/10.1007/BF00391276
BibTeX: Download - Kreimer, G., & Latzko, E. (1983). Properties of l-ascorbate-using peroxidases from Pisum sativum L. Hoppe-Seyler's Zeitschrift für Physiologische Chemie, 364(9), 1165-1165.
BibTeX: Download
Beiträge in Sammelwerken
- Kreimer, G., Wakabayashi, K.-i., Hegemann, P., & Dieckmann, C. (2023). The eyespot and behavioral light responses. In Dutcher S.K. (Eds.), The Chlamydomonas Sourcebook. (pp. 391-419). Elsevier Academic Press.
BibTeX: Download - Böhm, M., & Kreimer, G. (2020). Orient in the World with a Single Eye: The Green Algal Eyespot and Phototaxis. In Progress in Botany. (pp. 259-304). Cham: Springer.
BibTeX: Download - Kreimer, G. (2001). Light reception and signal modulation during photoorientation of flagellate green algae. In Donat-P. Häder and A.M. Breure (Eds.), Photomovement. (pp. 193-227). Amsterdam, London, New York, Oxford, Paris, Shannon, Tokyo: Elsevier.
BibTeX: Download - Kawai, H., & Kreimer, G. (2000). Sensory mechanisms: Light perception and taxis in algae. In Barry S. C. Leadbeater, John C. Green (Eds.), The Flagellates: Unity, Diversity and Evolution. (pp. 124-146). London and New York: Taylor & Francis.
BibTeX: Download - Kreimer, G. (1994). Cell Biology of Phototaxis in Flagellate Algae. In International Review of Cytology. (pp. 229-310). Academic Press Inc Ltd.
BibTeX: Download - Melkonian, M., Burchert, M., Kreimer, G., & Latzko, E. (1990). Binding and possible function of calcium in the chloroplast. In D.D. Randal and D.G. Blevins (Eds.), Current Topics in Plant Biochemistry and Physiology. (pp. 38-46). Interdisciplinary Plant Biochemistry and Physiology Program, University of Missouri-Columbia.
BibTeX: Download - Burchert, M., Surek, B., Kreimer, G., & Latzko, E. (1990). Calcium binding by chloroplast stroma proteins and functional implications. In Robert Thomas Leonard, Robert K. Hepler (Eds.), Calcium in plant growth and development: proceedings, 13th Annual Riverside Symposium in Plant Physiology. (pp. 17-25). American Society of Plant Physiologists.
BibTeX: Download - Latzko, E., Surek, B., & Kreimer, G. (1988). Calcium binding by stromal proteins and functional implications. In S. Vaklinova, V. Stanev and M. Dilova (Eds.), International Symposium on Plant Mineral Nutrition and Photosynthesis. (pp. 79-93).
BibTeX: Download - Kreimer, G., Surek, B., Heimann, K., Burchert, M., Lukow, L., Holtum, J.A.M.,... Latzko, E. (1987). Calcium metabolism in chloroplasts and protoplasts. In J. Biggins (Eds.), Proceedings of the 7th International Congress on Photosynthesis. (pp. 345-357). Dordrecht: Martinus Nijhoff Publishers.
BibTeX: Download - Latzko, E., Surek, B., & Kreimer, G. (1986). Ca2+ fluxes across the chloroplast envelope and Ca2+ binding by stromal proteins. In M. Gibbs (Eds.), Hungarian-USA Binational Symposium on Photosynthesis. (pp. 127-135).
BibTeX: Download

(Enlarge)

(Enlarge)

(Enlarge)

(Enlarge)

(Enlarge)

(Enlarge)

(Enlarge)

(Enlarge)

(Enlarge)

(Enlarge)

(Enlarge)

(Enlarge)











